化学療法の治療方針決定の指針となるオンコタイプDX乳がん再発スコア®プログラム
注)オンコタイプDX乳がん再発スコアプログラムは、オンコタイプDX乳がん再発スコア検査と日本向けに開発したソフトウエアを組み合わせたプログラム医療機器です。ここでは、オンコタイプDX乳がん再発スコア検査について概説します。
4つの主要な国際ガイドラインに採用され、欧州の2つの主要な医療技術評価機関に推奨されているオンコタイプDX乳がん再発スコア検査
TAILORx試験の結果に基づき、複数のガイドラインおよび医療技術評価機関の推奨は、オンコタイプDX乳がん再発スコア検査を望ましい検査として位置付けています2-6。全米総合がん情報ネットワーク®(NCCN®)は、RxPONDER試験1の最初の結果に基づき、オンコタイプDX乳がん再発スコア検査を推奨しています。
NCCN腫瘍学臨床診療ガイドライン(NCCNガイドライン®)が、術後化学療法の効果を予測できると認める検査であり、ホルモン受容体陽性、HER2陰性乳がんでリンパ節転移陰性および閉経後のリンパ節転移陽性(転移リンパ節1~3個)患者さんに対する「望ましい」多遺伝子検査に分類される検査1
TAILORx試験の結果により、オンコタイプDX乳がん再発スコア検査は、リンパ節転移陰性の早期浸潤性乳がん患者さんにおける術後化学療法の治療方針決定の指針となる十分なエビデンスを備えた検査と評価2
リンパ節転移陰性及び微小転移性早期乳がんの患者さんにおける化学療法の効果を予測できると考えられ、それ故、費用効果の高い選択肢となる検査3
リンパ節転移陰性および陽性の早期乳がんにおける術後化学療法の治療方針決定の指針として認識されている検査。リンパ節転移陰性の患者さんにおける治療方針決定の指針としてTAILORx試験のカットオフ値を使用4。
ER陽性、HER2陰性、早期乳癌のリンパ節転移陰性と閉経後のリンパ節転移陽性患者全てに強く推奨されている。臨床的リスクに関係なく推奨され、エビデンスの質も高い5
病理学的評価の補足となり、かつ術後化学療法の効果を予測する1Aエビデンスを備えた追加的予後予測及び/又は効果予測情報を得るために使用することができる6
a 全米総合がん情報ネットワーク® (NCCN®) は、NCCNの登録商標です。ASCOおよびESMOは、それぞれ米国臨床腫瘍学会および欧州臨床腫瘍学会の商標です。NCCN、英国国立医療技術評価機構(NICE)、ザンクトガレン国際コンセンサスパネル、ASCOおよびESMOは、いかなる製品および治療法についても保証をするものではありません。
b 2019年のザンクトガレン国際専門家コンセンサスパネルの大多数が投票したことによります。
乳がんに関するNCCNガイドラインがリンパ節転移陰性および陽性(N1)のホルモン受容体陽性、HER2陰性早期乳がんに対する21遺伝子検査(オンコタイプDX)を支持1,*,**
NCCN
ガイドライン
リンパ節転移陰性
オンコタイプDX乳がん再発スコア検査は、術後化学療法の効果を予測できる検査であり、リンパ節転移陰性患者さんに対する「望ましい」検査と認められています。
- オンコタイプDX乳がん再発スコア(21遺伝子)検査は、NCCNガイドラインにより術後化学療法の効果を予測できると認められ、リンパ節転移陰性のホルモン受容体陽性、HER2陰性乳がん患者さんに対する「望ましい」多遺伝子検査として分類された検査です。
- オンコタイプDX乳がん再発スコア®(21遺伝子)検査は、NCCNのリンパ節転移陰性アルゴリズムにおいて「強く考慮」するべき検査に引き上げられています。
- NCCNガイドラインは、化学療法に適するリンパ節転移陰性乳がん患者さんを選別するため、TAILORx試験に基づく21遺伝子検査の再発スコアカットオフ値を採用しています。
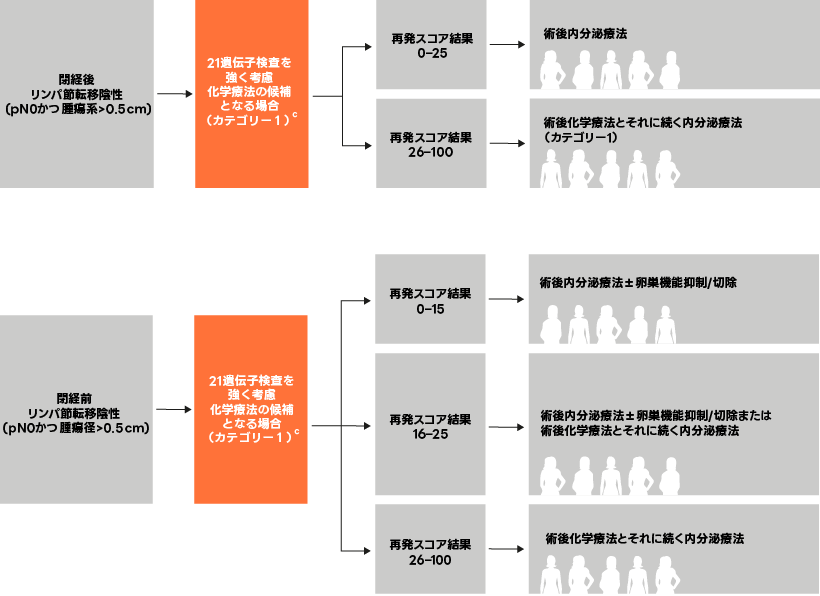
c.組織学的に低悪性度でリンパ管浸潤のないT1b腫瘍はTAILORx試験で対象とされなかったため、このような患者さんは内分泌療法単独で治療されるべきです。
NCCN
ガイドライン
転移リンパ節
1~3個
オンコタイプDX乳がん再発スコア検査は、閉経後のN1(転移リンパ節1~3個)患者さんにおける術後化学療法の効果を予測できる検査であり、「望ましい」検査と認められています。
- オンコタイプDX乳がん再発スコア(21遺伝子)検査は、NCCNガイドラインにより術後化学療法の効果を予測できると認められ、閉経後のN1(転移リンパ節1~3個)患者さんに対する「望ましい」多遺伝子検査として分類された検査です。
- NCCNは、オンコタイプDX乳がん再発スコア(21遺伝子)検査を閉経後のN1患者さんに対して「強く考慮」することを推奨しています。
- オンコタイプDX乳がん再発スコア(21遺伝子)検査は、閉経前のN1患者さんに対しても考慮するべきとされています。
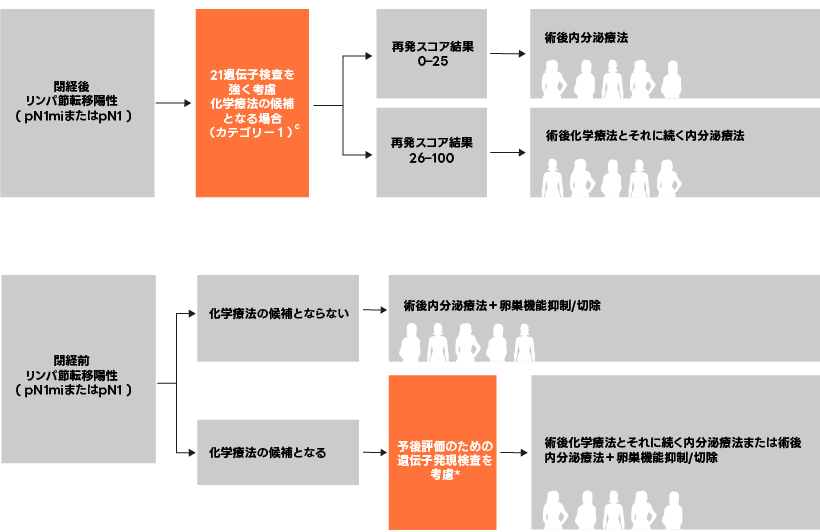
c 組織学的に低悪性度でリンパ管浸潤のないT1b腫瘍はTAILORx試験で対象とされなかったため、このような患者さんは内分泌療法単独で治療されるべきです。
* 再発スコア®結果が0~25の閉経前の患者さんにおいては、内分泌療法に化学療法を追加することにより、内分泌療法単独と比較して遠隔再発率が低下しましたが、この効果が化学療法によって促された卵巣機能抑制作用によるものかどうかは明らかではありません1。
全米総合がん情報ネットワーク®(NCCN®)は、NCCNの登録商標です。ASCOおよびESMOは、それぞれ米国臨床腫瘍学会および欧州臨床腫瘍学会の商標です。
NCCN、英国国立医療技術評価機構(NICE)、ザンクトガレン国際コンセンサスパネル、ASCOおよびESMOは、いかなる製品および治療法についても保証をするものではありません。
** NCCN腫瘍学臨床診療ガイドライン(NCCNガイドライン®)乳がん第5版(2021年)から許可を得て改変転載(©2021 National Comprehensive Cancer Network, Inc. All rights reserved)。ここに記載のNCCNガイドライン®および図解は、NCCNの特別許可を受けることなく、いかなる目的でもいかなる形式においても複製することを禁じます。NCCNガイドラインの最新完全版を見るには、オンラインで NCCN.org をご覧ください。NCCNガイドラインについては常に作業が進められており、新たな重要なデータが得られるたびに更新されることがあります。NCCNは、いかなる製品および治療法についても保証をするものではありません。NCCNは、それらの内容、使用または適用に関していかなる種類の保証を行うものではなく、どのような方式でもそれらの適用または使用に対して責任を負うものではありません。
化学療法に無作為化された50歳以下の女性において、遠隔転移がより少なかったことを示したTAILORx試験の探索的解析に基づき、再発スコア結果が16~25で50歳以下の女性においては術後化学療法の使用を考慮するようにしてください。前向き試験の副次的解析は、オンコタイプDX乳がん再発スコア検査が、腋窩リンパ節転移が1~3個の女性における化学療法の効果を予測できることを示唆しています。化学療法の効果を予測できることが証明されている多遺伝子検査は他にありません。
ドイツの医療技術評価機関であるIQWiG(医療品質・効率研究所)が、オンコタイプDX乳がん再発スコア®検査を化学療法の治療方針決定の指針として支持する勧告を発表2,7
オンコタイプDX乳がん再発スコア検査は、ホルモン受容体陽性、HER2陰性、リンパ節転移陰性の早期乳がんに対して術後化学療法を使用するか否かを決める指針として役立つエビデンスを備えた検査
- オンコタイプDX検査は、化学療法を回避できる女性とできない女性を識別することができます。
- 他の検査は類似性がないため、IQWiGによるアセスメントの結果は、当てはまりません。
- TAILORx試験では臨床的リスク評価が特に信頼できないものであることが示されていることから、臨床での意思決定に対するその役割りをよりよく理解する必要があります。
- 臨床的リスク評価により治療方針に確信を持てないすべての患者さんに検査を実施するべきです。
IQWiGについて
IQWiGは、世界で最も評判が高い医療技術評価機関の一つです。IQWiGは質の高い試験(最高レベルのエビデンスを備えた1A試験とみなされるもののみ)を重視し、臨床の結果に基づいた付加価値に関する主要な評価に重点的に取り組んでいます。IQWiGの推奨は、ドイツにおける公的費用償還に関するG-BA(ドイツ連邦合同委員会)の最終決定の指針となっています。
英国の医療技術評価機関であるNICEがオンコタイプDX乳がん再発スコア検査に関する推奨を拡大3
オンコタイプDX乳がん再発スコア検査は、リンパ節転移陰性だけでなく微小転移のある早期乳がんにも推奨されています。
- 化学療法の効果を予測できると考えられ、それ故、費用効果の高い選択肢となる検査
- 微小転移がある患者も使用対象とするよう、推奨が拡大
TAILORx試験によりオンコタイプDX乳がん再発スコア検査に関するエビデンスが大幅に追加されましたd。
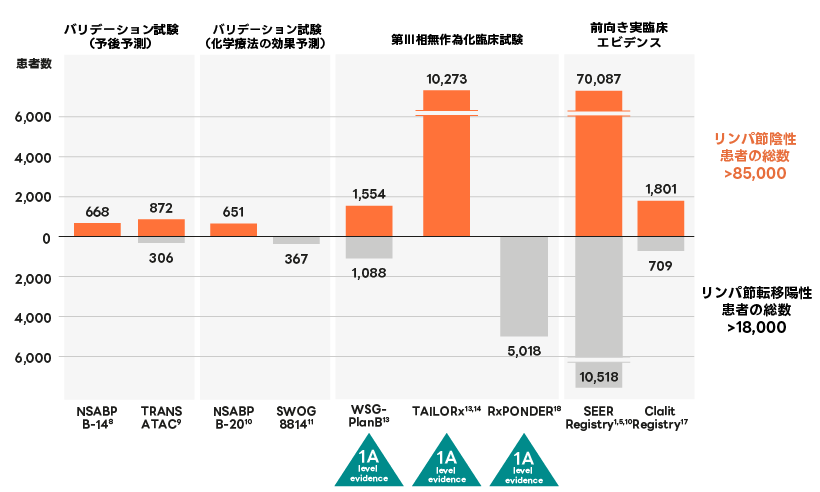
d ホルモン受容体陽性、HER2陰性、N0(リンパ節転移陰性)、N1(リンパ節転移1~3個)の早期乳がん患者さんについて。
-
リファレンス
